慢性肾脏病 (CKD)可发展为肾纤维化和终末期肾病,患者需要透析甚至肾移植。目前临床上暂无特效药,常用药物肾脏分布无特异性,剂量大副作用大,研发肾靶向递药系统意义重大。
学院张凌研究员团队研究发现,仿生高密度脂蛋白纳米粒是一种理想的肾小管靶向递药系统,可通过肾损伤分子-1(KIM-1)介导的内吞作用选择性被受损肾小管上皮细胞摄取而在受损肾小管蓄积。肾损伤分子是一种特异性高,表达于受损肾小管上皮细胞的磷脂酰丝氨酸受体,其表达水平与损伤程度正相关,是受损肾小管上皮细胞靶向递送的特异性靶点。
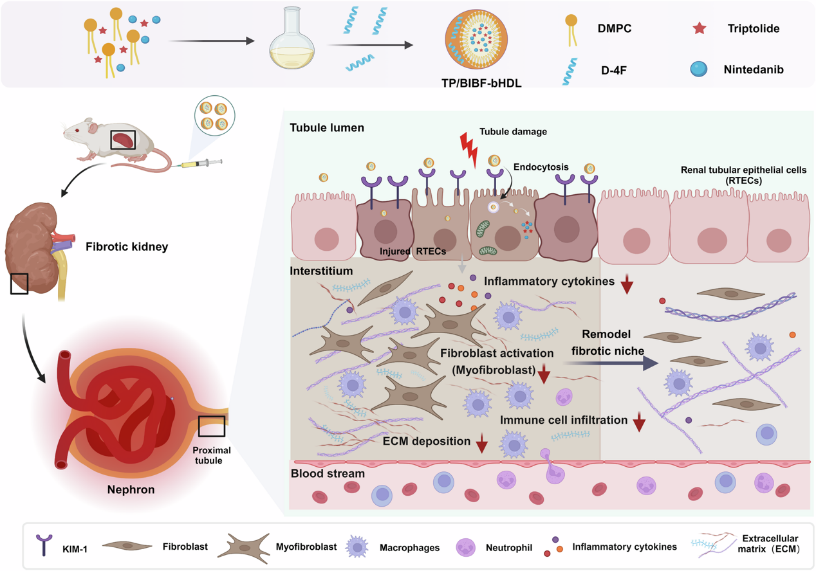
基于此发现,研究团队利用仿生高密度脂蛋白纳米粒共递送抗炎药物雷公藤甲素与抗纤维化药物尼达尼布到受损肾小管进行慢性肾病治疗。实验结果显示,共递送仿生高密度脂蛋白纳米粒能够有效减少免疫细胞浸润,抑制炎症因子的产生,并减少细胞外基质的合成,通过多靶点作用重塑肾脏纤维化微环境,从而有效抑制纤维化,延缓慢性肾病进展。与其他肾脏靶向载体相比,仿生高密度脂蛋白纳米粒具有以下优势:1)粒径小,具有克服肾小球滤过屏障的潜力;2)对受损肾小管上皮细胞具有选择性,无需表面靶向肽修饰;3)良好的生物相容性,不是血液清除的主要对象,也不容易受到蛋白冠附着影响;4)载体由磷脂和载脂蛋白模拟肽构建,组成简单且安全性高,具有较高的可制造性。
该成果为治疗CKD的靶向新药研发奠定了科学基础,具有重要科学价值和临床转化潜力。研究成果发表于高影响力学术期刊Nature Communications,题为“High-density lipoprotein nanoparticles spontaneously target to damaged renal tubules and alleviate renal fibrosis by remodeling the fibrotic niches”。4008com云顶集团2021级博士研究生贺珊珊为论文的第一作者,张凌研究员为论文的通讯作者。本研究受国家自然科学基金区域创新发展联合基金(No.U20A20411和No.U23A20495)以及国家重点研发计划(No.2023YFC2509302)的支持。
原文链接:https://www.nature.com/articles/s41467-025-56223-z#author-information.
DOI:https://doi.org/10.1038/s41467-025-56223-z.
撰稿:贺珊珊
编辑;杨燕玲
审核:李乙文