炎症性肠病(IBD)是一种慢性、反复发作的胃肠道炎症性疾病,包括克罗恩病和溃疡性结肠炎。IBD大大增加了罹患结直肠癌的风险,给全球数百万患者带来了终生的医疗负担。肠道微生物群的平衡与肠道健康息息相关。口服益生菌、抗生素、细菌代谢物和益生元补充剂已被证明可以影响肠道菌群。然而,由于消化道结构复杂、存在消化液以及这些物质的非靶向性,它们对结肠炎症中细菌的作用效果大打折扣,如何实现靶向结肠炎症有效调节肠道菌群是结肠炎症治疗领域的一项挑战。

近日,杨伟教授团队开发了基于纳米凝胶的多级NO释放微胶囊,利用NO的抗菌性实现对于肠道菌群的调节,从而减轻炎症和促进肠道屏障修复。微胶囊能够保护纳米凝胶耐消化液到达结肠部位,纳米凝胶通过透明质酸与CD44作用靶向结肠炎症,原位反应释放NO抑制致病菌的生长,增加益生菌的数量。肠道益生菌的增加促进短链脂肪酸和吲哚衍生物的产生,通过激活白细胞介素-17(IL-17)和PI3K-Akt信号通路调节肠道免疫力并恢复肠道屏障。相关工作以“A Gas Therapy Strategy for Intestinal Flora Regulation and Colitis Treatment by Nanogel-Based Multistage NO Delivery Microcapsules”为题发表在Advanced Materials,论文的第一作者为博士研究生傅雅君,通讯作者为杨伟教授和赵星博士后。该研究得到国家自然科学基金(NNSFC 52125301)、四川省自然科学基金(NSFSC 2023NSFSC1584)、4008com云顶集团材料Med-X中心Med-X创新计划(批准号:MCM202305)和4008com云顶集团博士后跨学科创新基金(批准号:JCXK2202)的资助。
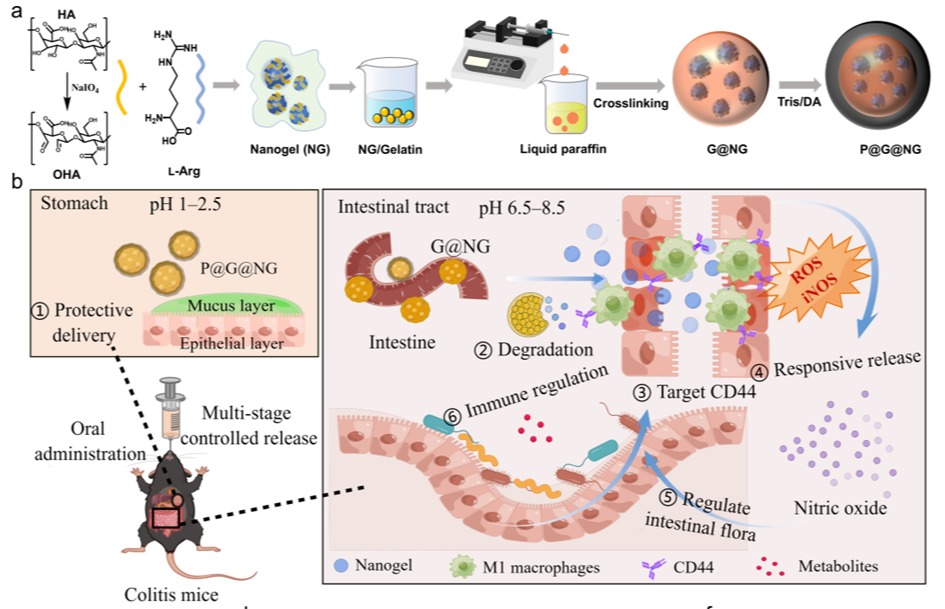
图1.基于纳米凝胶的多级NO递送微胶囊的设计和制造
微胶囊必须能够抵抗恶劣的胃肠道环境,以实现在不同消化液中的多级降解递送NO。通过体外消化液模拟多级NO递送微胶囊口服给药后在胃肠道中的降解性。聚多巴胺涂层包覆的微胶囊在不同消化液处理后形貌以及模量都比较稳定,能够抵御胃酸和胆碱。经多级NO递送微胶囊治疗的结肠炎小鼠结肠损伤程度与疾病组相比显著改善。
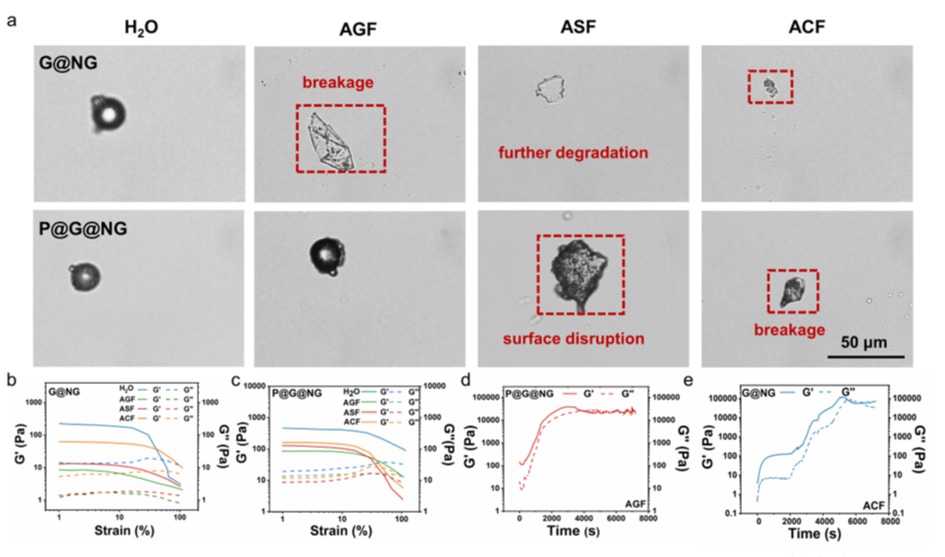
图2.多级NO递送微胶囊的多级消化液降解性
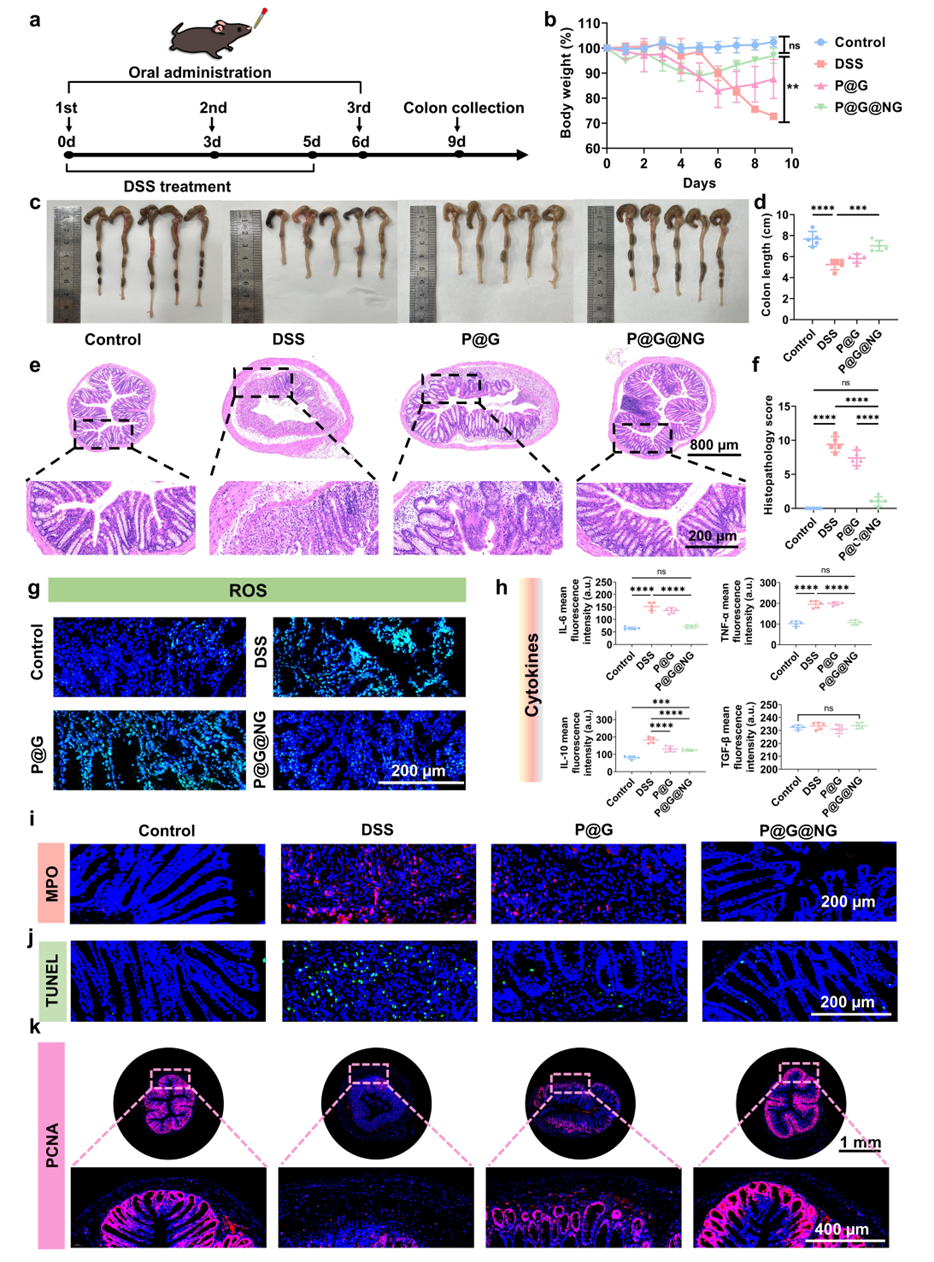
图3.多级NO递送微胶囊预防治疗结肠炎
肠道微生物群及其引起的代谢物组成的变化已被证明在肠道免疫调节与粘膜修复中具有至关重要的作用。16S rRNA测序技术、宏基因组学以及代谢组学分析结果表明NO的释放能够减少致病菌的丰度并且增加与抗炎和修复相关的细菌代谢物的产生。应用RNA-seq技术从基因水平分析NO调控菌群对肠道免疫的影响,多级NO递送微胶囊治疗组的小鼠与疾病小鼠的基因表达存在显著差异。基因本体分析表明,上调的基因与肠上皮细胞的增殖和分化有关,下调的基因与炎症、免疫和信号释放有关。对差异表达基因的通路富集分析表明,多级NO递送微胶囊通过激活IL-17和PI3K-Akt信号,从而减轻炎症、调节免疫并促进肠上皮细胞的增殖和分化。

图4. NO释放对肠道菌群和代谢物结构的影响
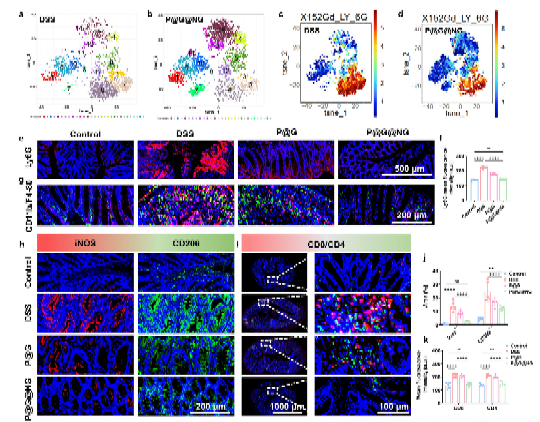
图5. 肠道微生物群和代谢物结构影响肠道免疫
原文链接:https://doi.org/10.1002/adma.202309972
撰稿:傅雅君
编辑:杨燕玲
审核:刘向阳